Врачам
5 февраля 2026
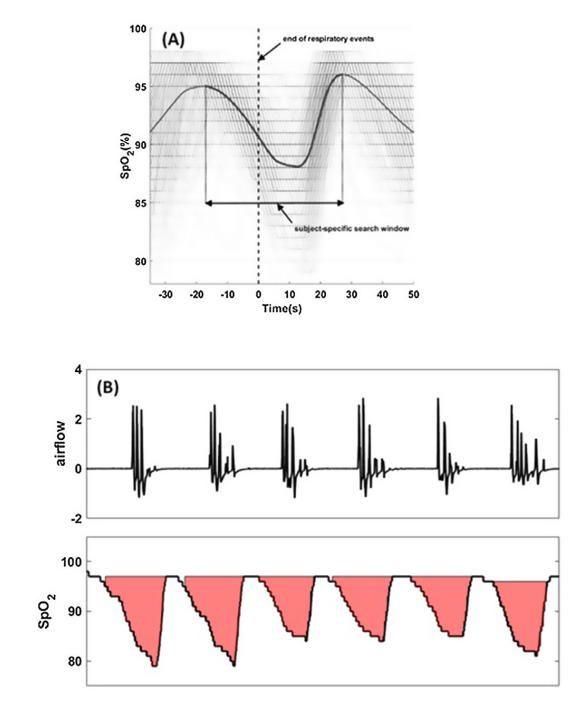
В данной обзорной статье обсуждаются методы количественной оценки гипоксической нагрузки, её характеристики, связь с клиническими исходами, а также ограничения данного показателя.
Миопатия Дюшенна — инвалидизирующее заболевание, которое со временем приводит к невозможности самостоятельно передвигаться и дышать без поддержки аппарата ИВЛ. Нередко из-за мышечной слабости, парезов и контрактур пациенты уже в 10-12 лет нуждаются в...
Дыхательная недостаточность — одна из ключевых жизнеугрожающих проблем при спинальной мышечной атрофии (СМА). Независимо от типа заболевания нарастающая слабость дыхательных мышц рано или поздно приводит к таким проблемам, как снижение эффективности ...
Искусственная вентиляция легких на дому — эффективный способ продлить жизнь пациентам с миопатией Дюшенна. Чаще всего она проводится неинвазивным способом в режиме BiPAP, хотя на поздних стадиях заболевания или при наличии бульбарного синдрома может ...
У каждого пациента с миопатией Дюшенна наступает момент, когда нужно задуматься о респираторной поддержке, а затем — об адаптации к аппарату ИВЛ.
Прогрессирующая слабость дыхательных мышц неизбежна при миопатии Дюшенна, но вспомогательная искусственная вентиляция легких положительным давлением позволяет улучшить перспективы пациентов.
20 января 2026
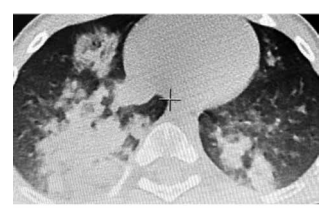
В статье представлены данные литературы и собственное клиническое наблюдение липоидной пневмонии у ребенка 2,6 года с тяжелой формой эпилепсии, детским церебральным параличом, дисфагией.
Детям с миопатией Дюшенна, к сожалению, уже в раннем возрасте может потребоваться специальный уход. Это генетически обусловленное заболевание характеризуется прогрессирующей мышечной слабостью, которая охватывает вначале проксимальную мускулатуру, а...
12 января 2026
Цель этого систематического обзора — оценить эффективность ИППВ как метода очистки дыхательных путей у пациентов детского возраста.