Врачам
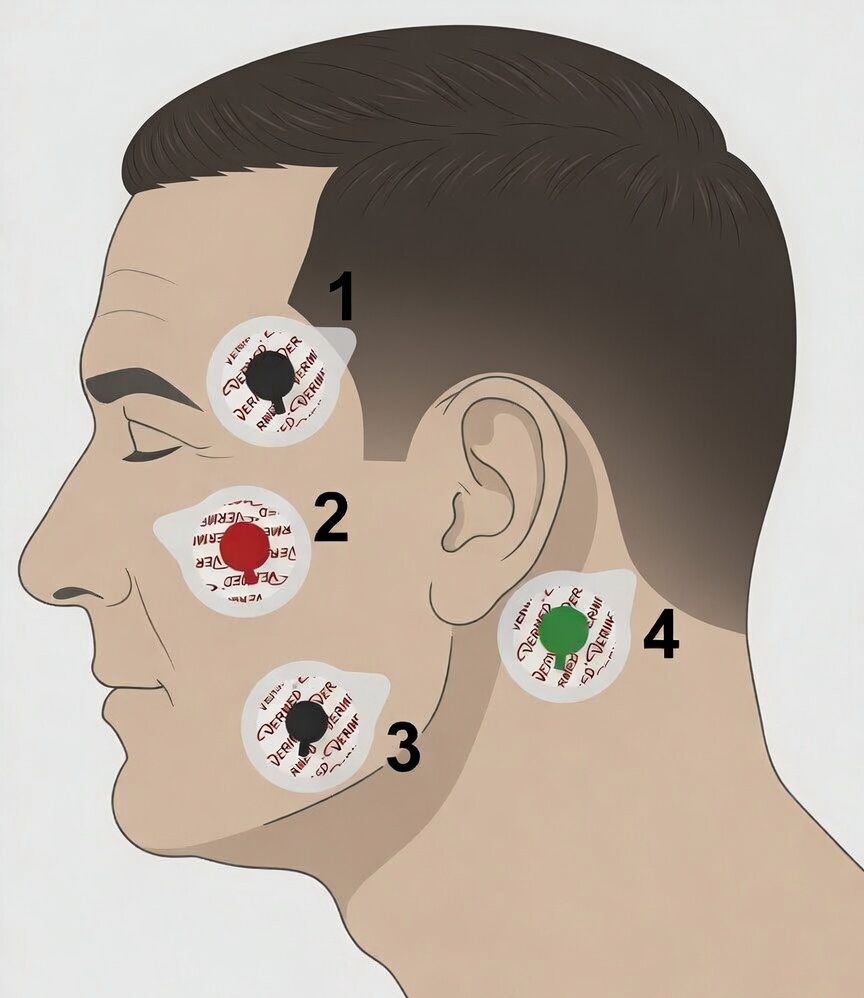
Современная диагностика нарушений сна выходит далеко за рамки выявления только апноэ. Нередко в клинической практике требуется комплексная оценка состояния пациента, включая такие состояния, как бруксизм и дисфункция височно-нижнечелюстного сустава &...
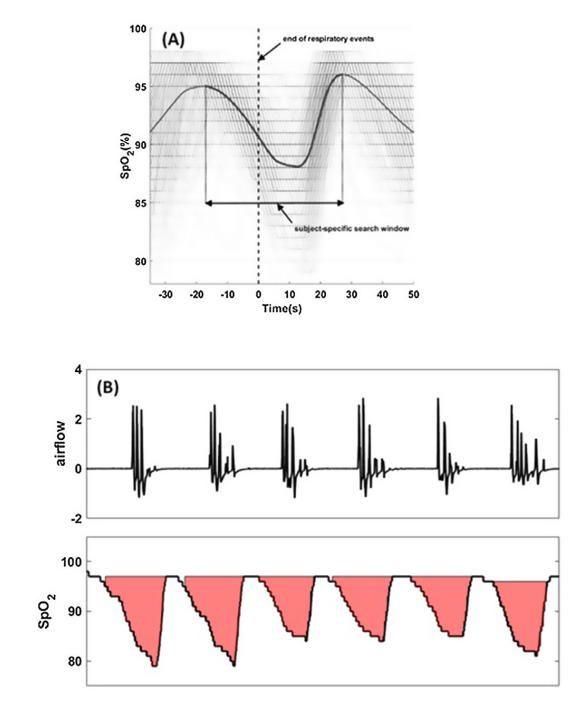
В данной обзорной статье обсуждаются методы количественной оценки гипоксической нагрузки, её характеристики, связь с клиническими исходами, а также ограничения данного показателя.
Главной целью данного исследования была оценка диагностической ценности устройства портативного мониторинга сна (ПМ) MediByte в сравнении с лабораторной ПСГ для педиатрической популяции.
Цели исследования: Целью данного мета-анализа является анализ согласованности определения индекса апноэ-гипопноэ (ИАГ) методами периферической артериальной тонометрии (ПАТ) и полисомнографии (ПСГ).
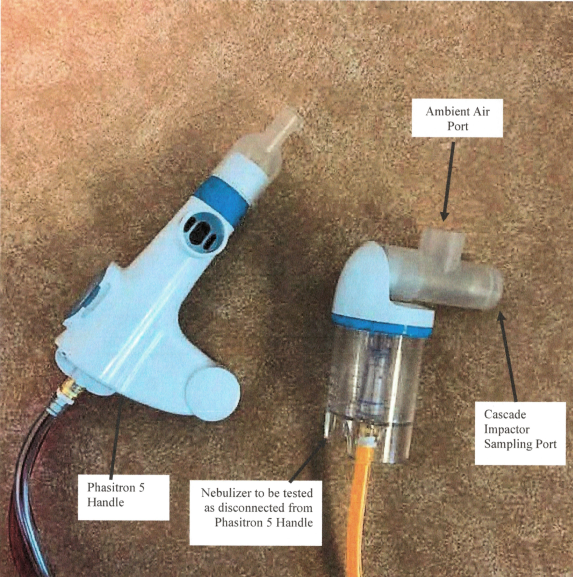
Результаты испытаний, проведенных лабораторией Piper Medical (Кармайкл, Калифорния, США) с целью оценки размера частиц и характера распыления лекарственных препаратов Небулайзером Фазитрона P5 компании Percussionaire.